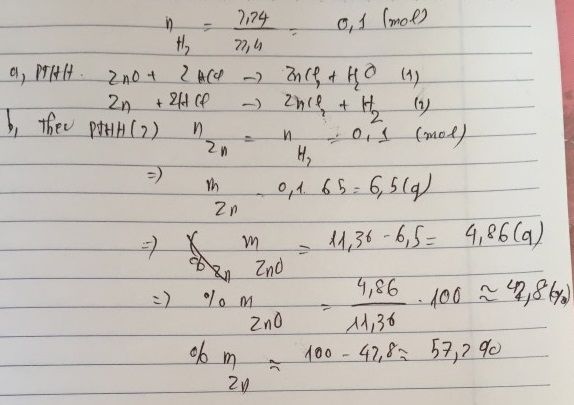Cho 1.5g hỗn hợp al, mỹ bằng dung dịch 7.3% thu được 1,68l khí
1. Tính khối lượng mỗi kim loại trong hũ ban đầu
2. Thích thể tích hcm cần dùng
Để hòa tan hoàn toàn 42.2 g hỗn hợp A gồm Zn và ZnO người ta phải dùng vừa đủ V(ml) để hcm 36.5%. Sau phản ứngthu được 8.96 lít khí
a. Xác định khối lượng mỗi chất có trong dung dịch A
b. Tính V
Tính thể tích khí clo thu được và thể tích hcm 4M cần dùng khi
a. Tác dụng với 8.7g MnO2
b. Tác dụng với 31.6g KMnO4